バイオテクノロジーの急速な進歩は、in vitro RNA合成技術によるmRNAワクチンの開発を通じて、COVID-19などの感染症との闘いに大きな影響を与えてきました。米国のModerna、ドイツのCureVac、ドイツのBioNTechなど、数多くの企業が治療用mRNAワクチンだけでなく、腫瘍、感染症、慢性疾患などの治療法も開発しています。
mRNAワクチンの研究と配合には、開発を成功させるために多様な原材料が必要です。分子酵素業界の先駆者として、
製品の品質と生産能力の両方を保証するために、
1. GMPの利点
2.
3. イェーセンは多くの製品でDMF番号を取得しました
4.
5.
6. 注文情報
1. GMPの利点
「GMP グレード」は、
表1. GMPの利点
| 品質管理 | 研究レベル | GMPグレード |
| 動物不使用 | 動物由来の材料が使用される場合がある | 必要に応じて動物不使用証明書を提供できます |
| 細胞バンクの特性評価 | それほど厳しくない | 厳格(GMP規制に準拠) |
| 原材料と完成品のトレーサビリティ情報 | それほど厳しくない | 厳格(GMP規制に準拠) |
| エンドトキシンレベルの制御 | / | 厳しい |
| 無菌管理 | / | 厳しい |
| 製造およびテストのバッチ記録 | それほど厳しくない | 厳格(必要に応じてバッチ記録を提供できます) |
| プロセス検証レポート | / | 必要に応じてレポートを提供することができます |
| 変更管理システム | 自己評価 | 厳格(GMP規制に準拠) |
| 品質管理システム | 自己評価 | ISO 13485認証 |
| DMF番号 | / | はい(報告) |
2. Yeasen はGMPグレードの製品を提供できます
3. イェーセンは多くの製品でDMF番号を取得しました
ドラッグマスターファイル (DMF) は、米国食品医薬品局 (FDA) に自主的に提出される機密文書です。このファイルには、ヒト用医薬品の製造、加工、包装、保管に使用される施設、プロセス、または物品に関する詳細な情報が記載されています。
FDA は、医薬品有効成分 (API) メーカーが新薬臨床試験申請 (IND)、新薬申請 (NDA)、新薬簡略申請 (ANDA)、または輸出申請をサポートするために DMF を参照する場合、DMF の技術的内容を精査します。DMF はこれらの申請で重要な役割を果たします。メーカーが特定の材料に対して DMF を提出すると、FDA の承認プロセスが大幅に迅速化されます。
4. Yeasen 製品の応用シナリオ
4.1 テンプレート生成
プラスミドの線形化は、プラスミドベクターを転写テンプレートとして使用する場合のテンプレート生成中に不可欠なステップです。転写が DNA テンプレートの末端まで進むと、プラスミドの線形化によって、定義された長さと配列の RNA 転写産物が生成されます。
4.2インビトロ転写(IVT)
インビトロ転写はさまざまな要因の影響を受けます。酵素、バッファー、修飾基質はすべて転写効率に大きな影響を与えます。
YEASEN Biotechは、ZymeEditorプラットフォームに基づいて、in vitro転写(IVT)プロセス中のdsRNAの生成を大幅に削減する新しいT7 RNAポリメラーゼを開発しました( T7 RNAポリメラーゼ、低dsRNA、250 U/μL )。これはmRNAの免疫原性を大幅に低下させ、ある程度までmRNAの完全性を高めます。この開発は、mRNAワクチンと癌治療薬の開発を進める上で重要な役割を果たすと期待されています。

バッファーを最適化し、ヌクレオチド基質の塩の種類を調整することで、転写の効率が大幅に向上し、dsRNAの生成が減少しました。

図2. Tris NTPはLVT効率を大幅に高め、dsRNAの生成を減らすことができる
4.3 mRNAキャッピング
5′ キャップ構造は免疫原性を低下させ、mRNA の効率的な翻訳に必要であるため、転写によって生成された mRNA の 5′ 末端にキャップ構造を追加する必要があります。
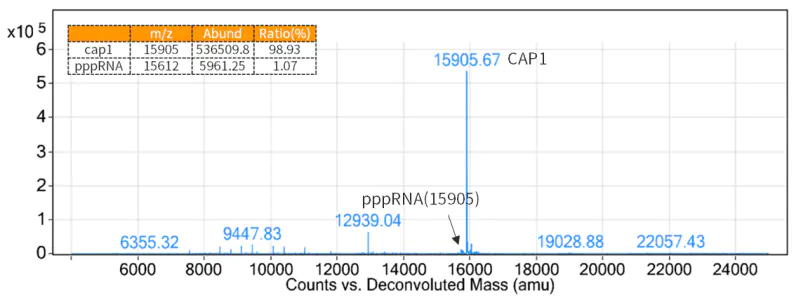
図3. キャップレート検出結果(LC-MS検出)
4.4 mRNAの精製
精製は、高純度の mRNA を実現するために不可欠なステップです。
5. Yeasen 社が提供するmRNAワクチン製造のための原材料
現在、
表2.
|
テンプレートの準備 |
インビトロ転写 |
||
|
10164ES |
10623ES |
||
|
10122ES |
10625ES |
||
|
10922ES |
10672ES |
||
|
10300ES |
10621ES |
||
|
|
10611ES |
||
| 10661ES |
10133ES |
||
| RNase R (20U/uL) | 14615ES |
10650ES |
|
|
シュバ1世 |
10662ES |
10651ES |
|
|
キャッピング |
精製 |
||
|
10614ES |
12602ES | ||
|
10612ES |
磁気分離ラック | 80460ES | |
|
10619ES |
36717ES |
||
|
10681ES |
|||
6. 注文情報
以下は
表3. 注文情報
読書に関して:
mRNA in vitro合成用GMPグレード試薬
DNase I とバイオメディカルにおける応用
参考文献:
[1] Chaudhary, N., Weissman, D., & Whitehead, KA (2021). 感染症に対するmRNAワクチン:原理、送達および臨床応用。ネイチャーレビュー。ドラッグディスカバリー、20(11), 817–838。
[2] Vogel, AB et al. 自己増幅RNAワクチンはインフルエンザに対してmRNAワクチンと同等の防御力を発揮するが、
はるかに低い用量で。分子療法:米国遺伝子治療学会誌26、446-455、
[3] Fuchs, AL, Neu, A. & Sprangers, R. 5'の迅速かつコスト効率の高い大規模生産のための一般的な方法
キャップドRNA。RNA(ニューヨーク、NY)22、1454-1466、doi:10.1261 / rna.056614.116(2016)。
[4] シュミット、A. 臨床試験用mRNAワクチン製造に関する考慮事項。分子生物学の方法(クリフトン、ニュージャージー州)1499、237-251、
[5] Banerji, A. et al. COVID-19疾患および報告されたアレルギー反応を予防するためのmRNAワクチン:最新のエビデンスと提案されたアプローチ。アレルギーおよび臨床免疫学ジャーナル。実践9、1423-1437、
[6] Richner, JM et al. 改変mRNAワクチンはジカウイルス感染を予防する。Cell 168, 1114-1125.e1110、
[7] コルベット、KS他「プロトタイプ病原体対策により可能になったSARS-CoV-2 mRNAワクチン設計」ネイチャー586、567-571、
[8] コルベット、KSら「mRNA-1273は非ヒト霊長類におけるSARS-CoV-2ベータ感染を防ぐ」ネイチャー免疫学22、1306-1315、
[9] Keech, C. et al. SARS-CoV-2組換えスパイクタンパク質ナノ粒子ワクチンの第1-2相試験。ニューイングランド医学ジャーナル383、2320-2332、
[10] クランプス、T. & エルバース、K. RNAワクチン入門。分子生物学の方法(クリフトン、ニュージャージー州)1499、1-11、
[11] Linares-Fernández, S., Lacroix, C., Exposito, JY & Verrier, B. 自然免疫と獲得免疫のバランスをとるmRNAワクチンの調整。分子医学の動向26、311-323、
